Длительность и эффективность воздействия различных лекарственных средств при патологических симптомах дентации у младенцев
Т.В. Казюкова, Л.И. Ильенко, В.К. Котлуков
— Кафедра факультетской педиатрии,
— кафедра госпитальной педиатрии № 2,
— кафедра поликлинической и неотложной педиатрии педиатрического факультета ФГБОУ ВО РНИМУ им. Н.И. Пирогова МЗ РФ, Москва, РФ
Проблема фармакотерапии при патологических симптомах дентации остается актуальной для специалистов во всем мире, поскольку на сегодня отсутствуют единые (кластерные) симптомы прорезывания зубов, нет единых подходов к ведению детей в этот сложный период жизни. Материалы и методы исследования: проведено открытое рандомизированное клиническое исследование (РКИ) по сравнительной оценке эффективности и безопасности двух лекарственных средств (ЛС) – Дантинорм Бэби и Калгель при прорезывании зубов у детей раннего возраста. 63 ребенка в возрасте от 6 мес до 2 лет 5 мес (33 мальчика и 30 девочек) составили две группы наблюдения. В 1-ю (основную) группу включен 31 (49,2%) ребенок (11,44±5,24 мес), которым при симптомах дентации закапывали в рот Дантинорм Бэби по 1 дозе 2–3 раза в день, в течение 3 дней. Во 2-ю группу (сравнения) вошли 32 (51,8%) ребенка (11,72±5,39 мес), которым при симптомах болезненной дентации родители втирали в участок десны гель Калгель не чаще 6 раз/сут в течение 3 дней. Длительность терапии – 3 дня, но не более 5 дней. Оценку состояния детей и симптомов дентации проводили в день обращения (визит 1), на 3–5-й день, после окончания терапии (визит 2) и на 6–8-й день (контрольный визит 3). Оценку симптомов проводили по 11 признакам. Осуществлялась также оценка эффективности лечения врачами и родителями по интегральной шкале IMOS, а также удовлетворенность лечением родителей детей по интегральной шкале IMPSS. Все результаты подверглись статистической обработке с помощью программы IBM SPSS Statistics 21.0.0. Результаты: во время визита 1 более чем у 75% детей обеих групп отмечались такие симптомы, как болезненность, зуд, отечность десен (p<0,001), слюнотечение (p<0,001), желание кусаться (p<0,001), раздражительность (p<0,001), снижение аппетита (p<0,001). На 3–5-й день терапии, в обеих группах число пациентов с патологическими симптомами дентации достоверно уменьшилось в сравнении с визитом 1 (p<0,05). Исключение составил учащенный стул у детей 2-й группы, получавших Калгель, показатель не имел достоверных отличий от визита 1 (p>0,05). При визите 3 симптомы дентации полностью купировались практически у всех детей обеих групп, но сохранялось раздражение кожи вокруг рта в 1-й группе (5) и 2-й группе (6), и учащенный стул у 4 детей 2-й группы (Калгель). В то время как в 1-й группе нарушений пищеварения не отмечалось (p<0,01), что обусловлено комплексным действием препарата Дантинорм Бэби. Обезболивающий/успокаивающий эффект, по оценке родителей, после приема Дантинорм Бэби наступал в среднем через 10,1±1,5 мин, а при нанесении геля Калгель – через 3,2±0,4 мин. Однако длительность воздействия 1 дозы Дантинорм Бэби в среднем составила 8,06±0,16 ч, что при 3-кратном приеме препарата обеспечивает непрерывную помощь при дентации 24 ч в сутки, в то время как действие геля Калгель длилось от 20 до 80 мин (60±8,5 мин). На 3–5-е сутки на фоне приема Дантинорм Бэби в 1-й группе симптомы прорезывания полностью купировались или значительно улучшились (83,9 и 90,4% – по оценке врачей и родителей). На фоне применения геля Калгель положительная динамика симптомов регистрировалась у 59,3% малышей, а по оценке родителей – в 43,7% случаев, что достоверно ниже показателей 1-й группы (p<0,001). Врачи и родители детей более высоко оценили эффективность терапии препаратом Дантинорм Бэби в сравнении с гелем Калгель (p<0,01). У 6 (18,8%) детей применение геля сопровождалось развитием нежелательных явлений на 2–3–4-й день терапии, что потребовало срочной отмены препарата. Заключение: доказана высокая клиническая эффективность и безопасность комплексного препарата Дантинорм Бэби, что позволяет рекомендовать его к практическому использованию для лечения патологических симптомов дентации.
Ключевые слова: дети раннего возраста, прорезывание молочных зубов, препараты для лечения патологических симптомов дентации, продолжительность воздействия и безопасность препаратов Дантинорм Бэби и Калгель.
Цит.: Т.В. Казюкова, Л.И. Ильенко, В.К. Котлуков. Длительность и эффективность воздействия различных лекарственных средств при симптомах патологической дентации у младенцев. Педиатрия. 2019; 98 (2): 133–140.
Прорезывание зубов – это уникальный процесс в развитии организма человека. В течение этого периода происходит процесс осевого (вертикального) перемещения зуба из места его закладки и развития (внутри челюсти) до появления зуба в полости рта. На прорезывание молочных зубов оказывают влияние различные факторы. Ряд исследователей считают, что основное значение в процессе дентации имеют генотип человека, его конституция [1], не исключается и роль внешне-средовых факторов.
Этиология или механизм, стоящий за прорезыванием, никогда не были полностью понятны. С позиций морфогенеза прорезывание зубов представляет собой сложный процесс, связанный с ростом и развитием зубов и альвеолярной кости, где одновременно происходят процессы резорбции и формирования кости. Насчитывается свыше 500 теорий и гипотез о механизмах прорезывания, не исключающих, а скорее дополняющих друг друга (корневая теория, сифонная, альвеолярная, ракетная, гормональная и др.) [2]. Среди врачей разных специальностей много десятилетий не прекращаются дискуссии относительно влияния симптомов, наблюдающихся в период дентации, на состояние здоровья младенцев [3–9]. Тем не менее «синдром прорезывания зубов» имеет свой код К00.7 в МКБ 10 [10] и включен в новую версию МКБ 11 [11]. Однако используется он довольно редко, поскольку диагноз правомочен только после исключения других возможных причин недомогания ребенка, совпадающих с периодом дентации.
Доподлинно не известно, что побуждает зуб к прорезыванию. Существует точка зрения, что во время дентации в организме ребенка происходит не столько естественная перфорация слизистой оболочки десен коронками, сколько повышенная выработка определенных гормонов, инициирующих гибель клеток в деснах, что освобождает место для нового зуба. Наиболее вескими считаются три теории дентации, выдвинутые еще в прошлом веке [2]:
1) т.н. «корневая» теория Хантера (J. Hunter), согласно которой растущие корни зуба упираются в твердое дно костной альвеолы, выталкивая зуб в ротовую полость;
2) Г.В. Ясвоин в «ракетной» теории объяснял механизм прорезывания зуба процессом дифференцировки мезенхимы зубного сосочка, что приводит к увеличению объема пульпы, которая создает давление внутри зубного зачатка, которое и движет его по направлению к краю альвеолы. Когда сосочек полностью превращается в пульпу, прорезывание завершается [12];
3) А.Я. Катц в «альвеолярной» теории дал более убедительное объяснение процессам дентации (1939). Он считал движущей силой прорезывания зубов одновременное воздействие нескольких процессов: перестройку костной ткани альвеолы вокруг развивающегося зуба, резорбцию и сопротивление альвеолы, напряжение в базальной части зачатка, функциональные раздражения (они возникают при жевании, и ведут к перестройке альвеолярной кости).
В последние годы появляются новые гипотезы о механизмах дентации. Так, G. Koch и S. Paulsen (2009) механизм дентации изложили следующим образом: «Прорезывание зубов сопровождается множественными изменениями тканей: резорбцией, наложением альвеолярной кости, развитием корня и пародонта. Процесс прорезывания определяется генетическими и местными факторами, в т.ч. «скученностью» среди развивающихся и прорезающихся зубов» [13]. Собственную гипотезу прорезывания описал I. Kjaer (2014), в соответствии с которой этот процесс находится в зависимости от трех основных факторов: 1) наличия свободного места на пути прорезывания зуба; 2) давления снизу на зачаток зуба; 3) адаптации зуба к периодонтальной связке (Periodontal Ligament) вокруг зуба, при помощи которой он крепится к кости [14].
Очевидно, что факт существования нескольких теорий прорезывания зубов, кратко рассмотренных выше, указывает на отсутствие единой теории, способной дать целостное объяснение многочисленным фактам, полученным в ходе изучения нормального развития зуба и его нарушений. Механизмы, постулируемые различными теориями, не являются взаимоисключающими, поскольку процесс дентации – многофакторный процесс, где сочетается действие нескольких механизмов [15]. В процессе развития зубочелюстной системы имеет значение также и комплекс других факторов, стимулирующих прорезывание, в частности нервная система. Пролиферация кости на дне зубной альвеолы и повышение внутрисосочкового давления служат важными факторами, способствующими продвижению зуба в вертикальном направлении. Но сами по себе они не могут служить достаточным объяснением механизма перемещения развивающегося зуба и не исчерпывают всех явлений, которые наблюдаются при дентации.
Ни одна из теорий не объясняет процессы перестройки и рассасывания кости в области альвеолярного отростка. По мнению А.Я. Катца (цит. по [2]), «эти процессы могут существенно усиливаться под влиянием функционального раздражения края десны, к примеру, различными твердыми предметами, которые ребенок охотно засовывает в рот в этот период (производя тем самым механическое раздражение десны), что способствует перестройке и рассасыванию кости». Прорезывание зуба – важнейший этап развития зубочелюстной системы, который протекает под воздействием нейрогуморальных влияний и внешне-средовых факторов и характеризуется трансформацией и ростом зубных и околозубных тканей [2].
Почему так много внимания мы уделили обсуждению механизмов прорезывания? На наш взгляд, ответ на этот вопрос позволит специалистам определить общие кластерные симптомы, характеризующие этот процесс. Понимание этиологии процесса дентации необходимо также для выработки стратегии по терапевтическому вмешательству в тех случаях, когда «курс прорезывания отклоняется от физиологического пути» [14].
Как свидетельствуют работы, где изучались симптомы прорезывания молочных зубов, примерно у 2/3 младенцев при дентации отмечаются дискомфорт и нарушение самочувствия, и лишь у 1/3 детей (счастливчиков) никаких отклонений в состоянии здоровья не наблюдается [4, 6, 9, 16–20].
На сегодня отсутствует единый взгляд на то, какие симптомы можно отнести к синдрому прорезывания, а какие следует исключить. Дети в период дентации часто становятся капризными, у них снижается аппетит, может повышаться температура тела, появляются насморк и кашель, изменяется характер стула [3, 4, 7, 9, 21]. Тем не менее, в ставшем «классическим» исследовании M.L. Macknin и соавт., в течение 7 месяцев наблюдавшие 125 детей (с 4 до 12 мес) своих коллег, сотрудников Кливлендской клиники (19 422 детских дней и 475 появившихся зубов), выделили «8-дневное окно прорезывания»: 4 дня до появления зуба, день прорезывания и 3 дня после [4]. Они также установили (уровень доказательности 2В), что с прорезыванием зубов достоверно связаны: желание кусаться, слюнотечение, повышение температуры тела (не выше 38 0С), высыпания на лице, плаксивость (для всех р<0,01). Авторы отметили, что такие симптомы, как диарея, кашель, рвота и повышение температуры тела >38,5 0С вероятнее всего вызваны инфекцией, и их не следует связывать с прорезыванием зубов [4].
Подъем температуры тела при дентации связан с выделением биологически активных веществ в зоне роста зуба, отмечается чаще накануне или в день прорезывания и длится не более 1–2 дней. Скопление слюны и повышенное выделение слизи в верхних отделах дыхательных путей реализуются влажным (обычно продуктивным) кашлем и ринореей, которые сохраняются в течение 3–5 дней. Кроме того, повышенное выделение слюны вызывает усиление перистальтики кишечника, что служит причиной более частого и/или разжиженного стула в течение 2–3 дней [4, 6, 22].
Таким образом, многие клинические проявления появляются одновременно с прорезыванием зубов, однако на сегодня невозможно определить четкие клинические признаки, патогномоничные для дентации, поскольку период прорезывания совпадает с периодом повышенного риска развития инфекций у грудных детей, что диктует необходимость исключения других причин недомогания ребенка.
В терапии патологической болезненной дентации применяют массаж десен, специальные резиновые кольца (грызунки), аппликации на десны местных анестетиков, а для снижения температуры тела, что улучшает общее состояние малыша, – такие лекарственные средства (ЛС), как парацетамол или ибупрофен. Частое применение этих ЛС может привести к нежелательным побочным и токсическим эффектам [23–26]. Более того, не всегда вышеперечисленные мероприятия дают желаемый результат.
Совершенствование фармакотерапии патологических симптомов при дентации у детей продолжает оставаться одной из наиболее актуальных задач педиатрической фармакологии. В практике детского здравоохранения в последнее время широко используются натуропатические ЛС, высокая эффективность и безопасность которых доказана как у нас в стране, так и за рубежом [1, 21, 27–30].
В более ранней нашей работе [21] также были доказаны высокая эффективность, безопасность и хорошая переносимость комплексного ЛС «Дантинорм Бэби» в сравнении со стоматологическим гелем «Калгель» в терапии симптомов болезненной дентации у младенцев. Вместе с тем, в рамках указанной статьи было уделено недостаточно внимания оценке длительности воздействия препаратов на симптомы патологической дентации.
Цель настоящей работы – провести сравнительный анализ длительности и эффективности воздействия препарата «Дантинорм Бэби» («Буарон», Франция) и стоматологического геля «Калгель» (ЗАО «ГлаксоСмитКляйн Трейдинг», Россия) у детей раннего возраста с патологическими симптомами дентации.
Материалы и методы исследования
Проведено открытое рандомизированное клиническое исследование (РКИ) по сравнительной оценке эффективности и безопасности двух лекарственных препаратов (Дантинорм Бэби и Калгель) при прорезывании зубов у детей раннего возраста. В состав стандартизованного препарата Дантинорм Бэби входят: Chamomilla vulgaris (ромашка), Phytolacca decandra (лаконос), Rheum (ревень). Основные компоненты геля Калгель: лидокаина гидрохлорид, цетилпиридиния хлорид.
Для участия в РКИ были рандомизированы 63 пациента в возрасте от 6 мес до 2 лет 5 мес (33 мальчика и 30 девочек). Полностью завершили РКИ 57 (90,5%) пациентов; 6 детей из группы сравнения выбыли из-за развития нежелательных явлений (НЯ).
Дети были распределены на две группы. В 1-ю (основную) группу включен 31 (49,2%) ребенок (Meвозр.=11,44±5,24 мес), которым при симптомах патологической дентации закапывали в рот раствор «Дантинорм Бэби» по схеме: по 1 дозе 2–3 раза в день, между кормлениями или приемами пищи, в течение 3 дней. Во 2-ю группу (сравнения) вошли 32 (51,8%) ребенка (Meвозр.=11,72±5,39 мес), которым при симптомах болезненной дентации родители наносили на десны гель Калгель по схеме: небольшое количество геля нанести на кончик пальца и осторожно втереть в воспаленный участок десны; гель при необходимости наносят повторно с интервалом не менее 20 мин, но не чаще 6 раз/сут, в течение 3 дней. Длительность применения сравниваемых ЛС в обеих группах составила 3 дня (min), но не более 5 дней (max).
Оценку состояния детей и симптомов дентации проводили в первый день обращения родителей по поводу симптомов болезненного прорезывания (визит 1), на 3–5-й день, после окончания терапии (визит 2) и на 6-й день (контрольный визит 3).
Симптомы дентации включали 11 признаков, каждый из которых оценивали по 3-балльной шкале (0 – отсутствует; 1 – слабо выражен; 2 – выражен умеренно; 3 – выражен максимально): 1) болезненность, зуд и/или отечность десен; 2) слюнотечение; 3) желание кусать/грызть предметы; 4) плаксивость, беспокойство; 5) нарушение аппетита; 6) нарушение сна; 7) повышение температуры тела (до 38 0С); 8) насморк; 9) кашель; 10) раздражение кожи вокруг рта, на лице, шее; 11) учащение или разжижение стула.
Оценка эффективности лечения осуществлялась врачами и родителями по интегральной шкале IMOS (Integrative Medicine Outcome Scale): 5 баллов – полное выздоровление, 4 – значительное улучшение, 3 – незначительное улучшение, 2 – состояние без изменений, 1 – ухудшение состояния, развившееся на фоне терапии, появление новых симптомов. Родители детей оценивали удовлетворенность проводимой терапией по интегральной шкале IMPSS (Integrative Medicine Patient Satisfaction Scale): 5 баллов – всецело удовлетворен, 4 балла – удовлетворен, 3 балла – отношусь нейтрально, 2 балла – не удовлетворен, 1 балл – крайне не удовлетворен.
Статистическая обработка результатов динамической оценки симптомов дентации проведена с помощью программы Statistica SPSS, версия 21.0. Для параметрических данных рассчитывали средние величины (M), стандартное отклонение (SD) и медиану (Me), для непараметрических показателей определяли различия между переменными с использованием непараметрического U-критерия Вилкоксона– Манна–Уитни), различия считали статистически значимыми при р<=0,05.
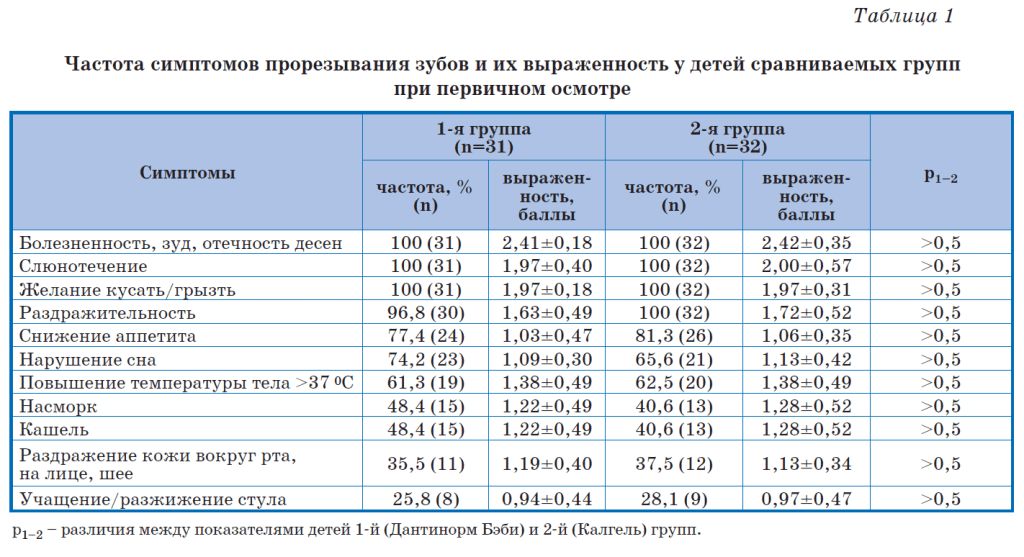
Результаты и их обсуждение Частота встречаемости симптомов прорезывания и их выраженность при первом обращении/осмотре не имели достоверных различий в сравниваемых группах (табл. 1). При первом визите самыми частыми симптомами (более чем в 75% случаев) были: болезненность, зуд, отечность десен (Me: 2,41, p<0,001), слюнотечение (Me: 2, p<0,001), желание кусать/ грызть (Me: 1,97, p<0,001), раздражительность (Me: 1,7, p<0,001), снижение аппетита (Me: 1,05, p<0,001), что согласуется с данными других авторов [4–9]. Во время визита 2, на 3–5-й день терапии, в обеих группах число пациентов с патологическими симптомами дентации достоверно уменьшилось (табл. 2). Как видно из табл. 2, в обеих группах на 3–5-й день наблюдения достоверно снизилась выраженность почти всех симптомов в сравнении с первым визитом (p<0,05). Исключение составил учащенный стул в группе сравнения: его выраженность (в баллах) у детей, получавших Калгель, не имела достоверных отличий от визита 1 (p>0,05). На 6–8-й день (визит 3) симптомы дентации полностью купировались практически у всех детей как в основной группе, так и в группе сравнения [21].
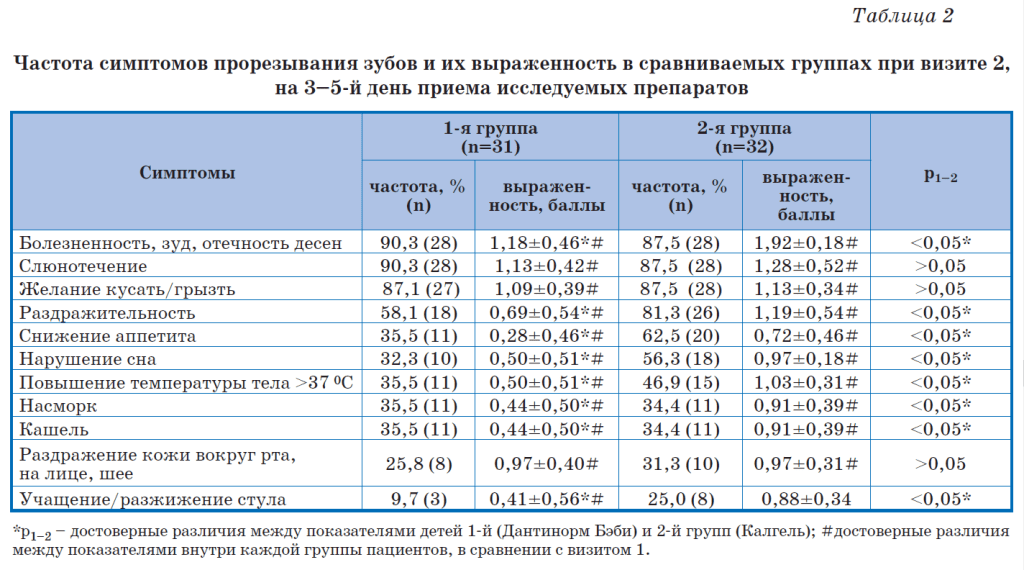
Вместе с тем на 6–8-й день наблюдения сохранялось раздражение кожи вокруг рта у 5 детей 1-й группы и у 6 детей 2-й группы (у всех зубы прорезались на 5-й день терапии). Кроме того, у 4 детей 2-й группы (Калгель) сохранялся учащенный стул, в то время как в 1-й группе нарушений пищеварения не отмечалось (p<0,01), что обусловлено комплексным воздействием компонентов препарата Дантинорм Бэби.
Таким образом, в ходе данного РКИ у 63 младенцев появились 68 молочных зубов, причем у подавляющего большинства (50 детей – 80,65%) – в первые 3–5 дней наблюдения: на 3-й день – у 7; на 4-й день – у 17, на 5-й день – у 26. У остальных 13 детей (19,35%) – на 6–7-й день наблюдения: на 6-й день – у 9, на 7-й день – у 4 малышей. Важнейшими клиническими аспектами применения ЛС, используемых при патологических симптомах дентации, являются быстрота наступления (через какое время после приема) обезболивающего или успокаивающего эффекта и его продолжительность.
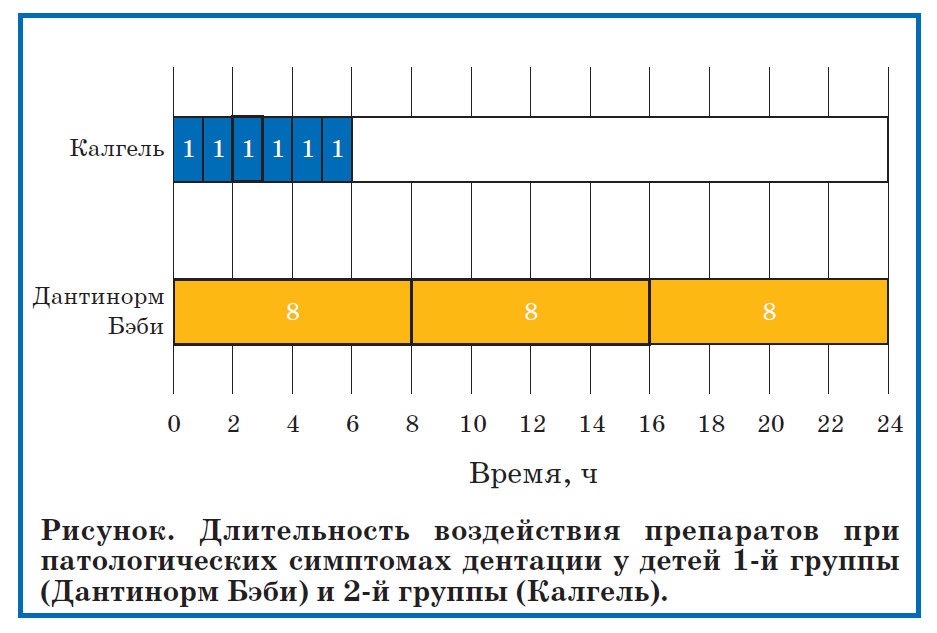
По оценке родителей, при нанесении геля Калгель обезболивающий эффект наступал через 3,2±0,4 мин, а его действие длилось 60±8,5 мин. После приема Дантинорм Бэби родители отмечали исчезновение у детей беспокойства, раздражительности, плаксивости через 10,1±1,5 мин, а продолжительность воздействия 1 дозы препарата в среднем составила 8,06±0,16 ч, таким образом, при 3-кратном приеме препарата обеспечивая непрерывную помощь при дентации 24 ч в сутки (см. рисунок).
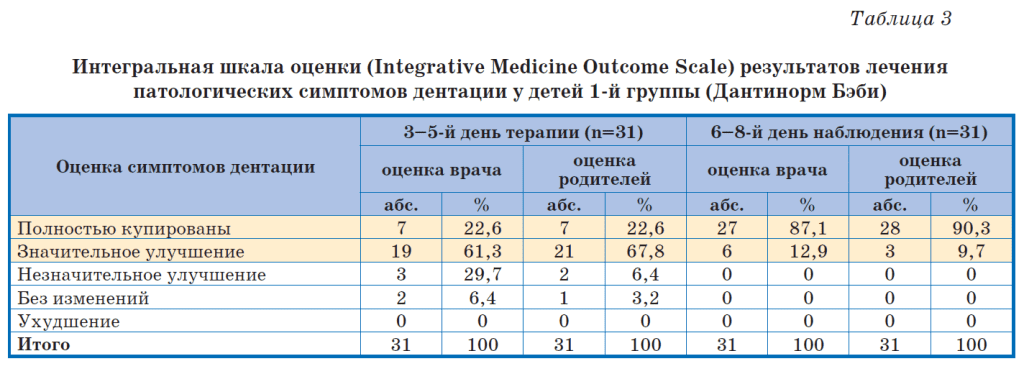
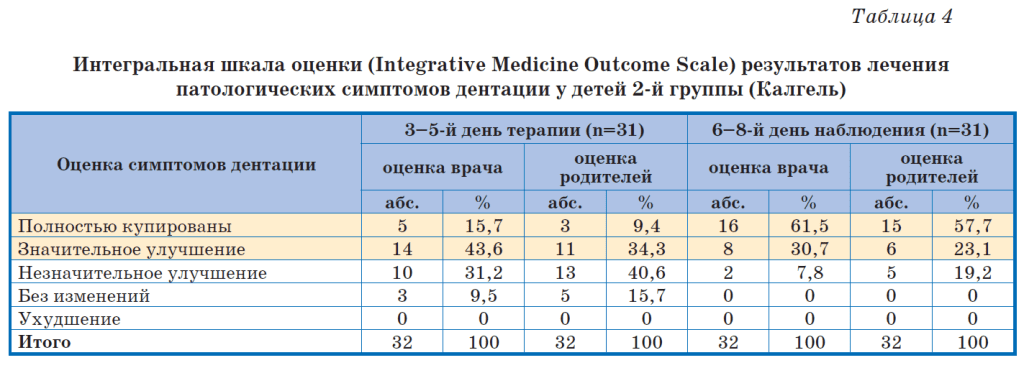
Оценка эффективности терапии, проведенная по интегральной шкале IMOS, раздельно – врачами-исследователями и родителями детей – представлена в табл. 3 и 4.
Как видно из приведенных данных, уже на 3–5-е сутки на фоне приема Дантинорм Бэби в 1-й группе симптомы прорезывания полностью купировались или значительно улучшились в 83,9 и 90,4% случаев соответственно по оценке врачей и родителей. В то время как во 2-й группе, где применяли Калгель, положительная динамика симптомов регистрировалась лишь у 59,3% малышей, а по оценке родителей – в 43,7% случаев, что достоверно ниже показателей 1-й группы (p<0,001). На 6–8-й день клинического мониторинга полное купирование симптомов или значительное улучшение зафиксировано практически у всех детей основной группы, как по оценке врачей, так и родителей. В группе сравнения полное купирование симптомов или улучшение наблюдалось в 92,2 и в 80,8% случаев соответственно по оценке врачей и родителей (p<0,01). Таким образом, врачи и родители дали более высокую оценку эффективности терапии комплексным препаратом Дантинорм Бэби по сравнению с гелем Калгель.
В педиатрической практике особые требования предъявляются к безопасности ЛС, которые регистрируются у пациентов вскоре после приема исследуемого препарата. Отмечают вероятность развития побочных эффектов или нежелательных явлений (НЯ): высоко вероятно, вероятно, маловероятно, не связано с приемом ЛС, и при необходимости назначают соответствующую терапию.
В нашем исследовании у 6 (18,8%) детей применение геля сопровождалось развитием НЯ на 2–3–4-й день терапии, что потребовало срочной отмены препарата. У 5 из 6 детей отмечены отек и гиперемия десен вскоре после нанесения геля (2–3-й день приема), у 3 – аллергическая сыпь на щеках и груди (3-й день приема), у 2 детей – отказ от еды (3-й день приема). У одного пациента отмечалось нарушение глотания (в условиях гиперсаливации представляет высокий риск аспирации), у одного – появление выраженной одышки, беспокойства и тахикардии через 5 мин после повторного нанесения геля (вероятно, из-за увеличения кратности его нанесения до 8 раз/сут). На наш взгляд, применение препарата Калгель, способного вызвать тяжелые осложнения, представляется неразумным. Как отмечает FDA (Food and Drug Administration), детские гели на основе лидокаина опасны из-за высокого риска развития побочных эффектов и угрожающих жизни состояний (судороги, нарушения сердечного ритма и др.), а предсказать проаритмогенный эффект лидокаина вообще довольно сложно. Соотношение вреда и пользы этих препаратов стало весомым аргументов для FDA при запрете на использование лидокаинсодержащих гелей (2014) [31].
Заключение
Симптомы дентации не являются специфичными, и к их оценке сегодня нет единого кластерного подхода. Вместе с тем почти 2/3 детей в этот период испытывают недомогание и другие патологические симптомы прорезывания. В настоящее время имеются эффективные и безопасные ЛС, в т.ч. на основе природных субстанций, помогающие справиться с этим нелегким периодом.
В нашем РКИ уже на 3-й день приема Дантинорм Бэби отмечено статически достоверное снижение выраженности клинических проявлений патологических симптомов дентации (p<0,05) – полное купирование (35,5%) или значительное улучшение (64,5%). В то время как в группе сравнения, где применяли Калгель, некоторые из симптомов дентации сохранялись достоверно дольше, до 6–8-го дня наблюдения (p<0,05).
По оценке родителей, после приема Дантинорм Бэби дети становились спокойнее в среднем через 10,1±1,5 мин. В отличие от стоматологического геля, обезболивающее действие которого длится в среднем 60±8,5 мин, продолжительность воздействия 1 дозы препарата Дантинорм Бэби в среднем составила 8,06±0,16 ч. Таким образом, прием 3 доз препарата обеспечивает непрерывную помощь при дентации 24 ч в сутки. При этом в первый же день приема у детей восстанавливался ночной сон, чего не наблюдалось при нанесении геля Калгель.
При симптомах патологической дентации, как правило, не встречается серьезных осложнений, в большей мере эту ситуацию переживают родители ребенка. Комплексный препарат Дантинорм Бэби идеально применим в период дентации, выпускается в жидкой форме, удобной для малышей. В отличие от многих других фитопрепаратов, он является стандартизованным лекарственным средством, создан на основе растительных субстанций (ромашки, лаконоса, ревеня). Препарат не имеет противопоказаний, не вызывает побочных и нежелательных явлений, не увеличивает фармакологическую нагрузку на растущий организм, почти 20 лет с успехом используется в европейских странах [30, 32, 33]. Результаты, полученные нами в ходе этого клинического сравнительного исследования, подтвердили высокую клиническую эффективность и безопасность препарата, что позволяет рекомендовать комплексный препарат Дантинорм Бэби к широкому использованию в ежедневной клинической практике для купирования патологических симптомов дентации.
Благодарности: авторы выражают признательность врачам и лично И.В. Панкратову, главному врачу ГБУЗ МО «Голицынская поликлиника», а также родителям детей, принявшим участие в исследовании и анкетировании.
Контактная информация:
Казюкова Тамара Васильевна – д.м.н., проф.
каф. факультетской педиатрии педиатрического
факультета ФГБОУ ВО РНИМУ им. Н.И. Пирогова
МЗ РФ
Адрес: Россия, 117997, г. Москва,
ул. Островитянова, 1
Тел.: (963) 711-61-93,
E mail: legacy_millenium@hotmail.com
Статья поступила 15.02.19,
принята к печати 25.03.19.
- Захарова И.Н., Холодова И.Н., Дмитриева Ю.А., Морозова Н.В., Мозжухина М.В., Холодов Д.И. Может ли физиологический процесс прорезывания зубов у младенцев быть патологическим? Медицинский совет. 2016; 1: 31–35.
- Детская терапевтическая стоматология: национальное руководство. В.К. Леонтьев, Л.П. Кисельникова, ред. М.: ГЭОТАР-Медиа, 2010: 896.
- Таточенко В.К. Педиатру на каждый день-2016: справочник по диагностике и лечению. 8-е изд. М.: ООО «Компания Боргес», 2016: 272.
- Macknin ML, Piedmonte M, Jacobs J, Skibinski C. Symptoms associated with infant teething: a prospective study. Pediatrics. 2000; 104: 747–752.
- Peretz B, Ram D, Hermida L, Otero MM. Systemic manifestations during eruption of primary teeth in infants. J. Dent. Child. 2003; 70: 170–173.
- Ramos-Jorge J, Pordeus IA, Ramos-Jorge ML, Paiva SM. Prospective longitudinal study of signs and symptoms associated with primary tooth eruption. Pediatrics. 2011; 128 (3): 471–476.
- Tighe M. Does a teething child need serious illness excluding? Arch. Dis. Child. 2007; 92: 266–273.
- Nemezio MA, De Oliveira KMH, Romualdo PC, Queiroz AM, Paula-e-Silva FWG, Silva RAB, Kuchler EC. Association between Fever and Primary Tooth Eruption: A Systematic Review and Meta-analysis. Int. J. Clin. Pediatr. Dent. 2017; 10 (3): 293–298.
- Клещенко Е.И., Жданова И А., Лукиша А.Н., Краковец И.В., Смычкова Е.В., Картавцева А.В. Симптомы прорезывания зубов у младенцев: состояние или болезнь? Кубанский научный медицинский вестник. 2017; 24 (4): 78–81.
- http://mkb-10.com/index.php?pid=10003
- http://mkb-11.com/
- Ясвоин Г.В. О механизме прорезывания зубов. Одонтология и стоматология. Л., 1929.
- Koch G, Poulsen S. Pediatric Dentistry. A Clinical Approach. Wiley-Blackwell, 2009.
- Kj?r I. Mechanism of human tooth eruption: review article including a new theory for future studies on the eruption process. Scientifica (Cairo). 2014: 341905.
- Быков В.Л. Гистология и эмбриология органов полости рта человека. Учебное пособие. 2-е изд. СПб.: Специальная литература, 1998: 248.
- Nelson textbook of pediatrics. Kliegman RM, Stanton BF, St Geme III JW, et al., eds. 20th ed. Philadelphia: Elsevier, 2016.
- Sood S, Sood M. Teething: myths and facts. J. Clin. Pediatr. Dent. 2010; 35 (1): 9–13.
- Peretz B, Ram D, Hermida L, Otero MM. Systemic manifestations during eruption of primary teeth in infants. J. Dent. Child. 2003; 70: 170–173.
- Memarpour M, Soltanimehr E, Eskandarian T. Signs and symptoms associated with primary tooth eruption: a clinical trial of nonpharmacological remedies. BMC Oral Health. 2015; 15: 88–92.
- Заплатников А.Л., Касьянова А.Н., Майкова И.Д. Синдром прорезывания зубов у младенцев: новый взгляд на старую проблему. Русский медицинский журнал. 2018; 5 (2): 68–71.
- Казюкова Т.В., Радциг Е.Ю., Панкратов И.В., Алеев А.С. Сравнение клинической эффективности и безопасности двух лекарственных препаратов в терапии симптомов прорезывания молочных зубов у детей раннего возраста («Дантинорм Бэби» vs «Калгель»). Педиатрия. 2018; 97 (1): 122–130.
- Tsang AKL. Teething, teething pain and teething remedies. Int. Dentistry SA. 2010; 12 (5): 48–61.
- Oman TK, Stewart MC, Burns A, Lang TF. Topical choline salycilates implicated in Reye’s syndrome. BMJ. 2008; 336: 1376.
- Williams GD, Kirk EP, Wilson CJ, Meadows CA, Chan BS. Salicylate intoxication from teething gel in infancy. Med. J. Aust. 2011; 194 (3): 146–148.
- Nguyen T, Cranswick N, Rosenbaum J, Gelbart B, Tosif S. Chronic use of teething gel causing salicylate toxicity. Paediatr. Child Health. 2018; 54 (5): 576–578.
- Hofer KE, Kaegi S, Weiler S. The acute toxicity profile of a teething gel containing salicylamide in toddlers: an observational poisons centre-based study. Clin. Toxicol. (Phila). 2018; 16: 1–2.
- Ильенко Л.И., Сырьева Т.Н., Холодов Д.И., Гайнова Л.В., Семашина Г.А. Использование средств природного происхождения при патологической дентации у детей первых лет жизни. Вопросы детской диетологии. 2011; 9 (2): 2–4.
- Студеникин В.М., Акоев Ю.С. Антипиретики/ анальгетики в современной педиатрии: аллопатия и гомеопатия. Лечащий врач. 2016; 6: 7–11.
- Taneja D, Khurana A, Vichitra A, Sarkar S, Gupta AK, Mittal R, Bawaskar R, Sahoo AR, Prusty U, Singh S, Sharma M, Pant R, Singh U, Upadhyay AK, Sehegal S, Patnaik S, Nath T, Manchanda RK. An assessment of a public health initiative of homeopathy for primary teething. Homeopathy. 2019; 108 (1): 2–11. doi: 10.1055/s-0038–1673650.
- Ip EJ, Patel P B, Chi J J, Shah-Manek B, Lau B. What are pharmacists recommending for infant teething treatment? J. Am. Pharm. Assoc. 2018; 58 (1): 79–83.
- FDA Drug Safety Communication: FDA recommends not using lidocaine to treat teething pain and requires new Boxed Warning. U.S. Department of Health and Human Services. 6-26-2014. https://www.fda.gov/Drugs/DrugSafety/ ucm402240.htm
- McIntyre GT, McIntyre GM. Teething troubles? BDJ. 2002; 192 (5): 251–255.
- Ekins-Daukes S, Helms PJ, Taylor MW, Simpson CR, McLay JS. Paediatric homoeopathy in general practice: where, when and why? Br. J. Clin. Pharmacol. 2014; 59 (6):743–749.
